Published: Feb 06, 2026
在合成生物学研究中,如何精确、灵敏地“感知”并“响应”外界信号,构建具有可预测功能的基因回路是实现细胞功能定制化改造的核心。尽管已有多种基因调控工具,如何在抑制泄漏表达的同时有效增强信号输出,仍是领域内的一大挑战。这类似于电子设备中兼具降噪与信号放大功能的低噪音放大器(Low noise amplifiers, LNAs)。双组分系统(Two-component systems, TCSs)是细菌控制生理代谢行为最为重要的信号感知通路,信号感知范围广、感知能力强,被视为开发高性能合成生物传感器的宝贵资源。然而,传统观点认为TCS的输出对胞内组分浓度变化具有鲁棒性,这一认知使TCS长期被视作难以精准调控的“黑箱”,从而严重限制了其在合成生物学中的深度开发与拓展应用。
近日,浙江大学王宝俊教授与华东理工大学叶邦策教授等联合研究团队在Cell子刊Cell Systems上发表了题为“Refactoring two-component systems for tunable gene expression regulation and upgraded bacterial sensing”的研究(浙江大学杭州国际科创中心陈升言副研究员与浙江大学物理高等研究院徐浩然研究员为论文共同第一作者,王宝俊教授、叶邦策教授与浙江大学杭州国际科创中心周楠研究员为论文共同通讯作者)。该工作通过系统性“重编程”,首次揭示了TCS核心元件——响应调节蛋白与组氨酸激酶可作为浓度依赖的“调控旋钮”,并在此基础上开发出可预测的基因表达调控工具与首个生物版“低噪音放大器”(图1),为工程菌在环境监测、活体诊疗和生物制造等领域的传感应用提供了全新技术支撑。
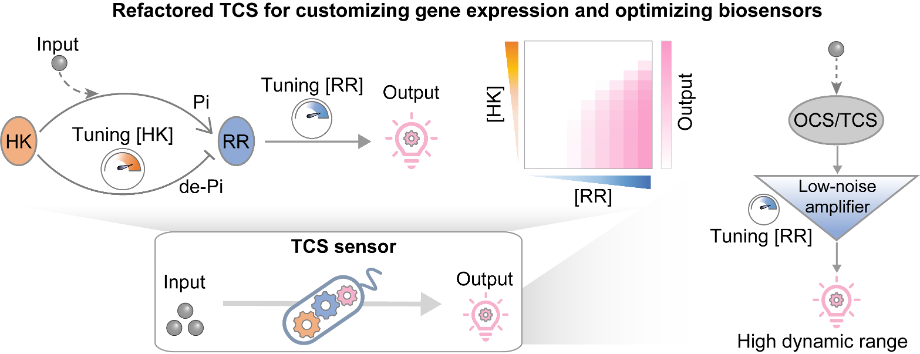
在微生物感知世界的“工具箱”中,单组分系统(OCS)与双组分系统(TCS)是最核心的两类信号通路,它们构成了设计合成生物传感器与复杂基因线路的基石。过去二十年,基于OCS的调控工具已被广泛开发与应用,而TCS——这个在细菌信号调控网络中综合占比高达26%的家族,其真正的潜力却长期被一个固有观念所束缚。即TCS的输出对其核心元件——膜上的“传感器”组氨酸激酶(HK)和胞内的“效应器”响应调节蛋白(RR)的浓度变化不敏感,具有鲁棒性。这一观念使得TCS在可编程基因调控方面的潜力长期被忽视。
为真正释放TCS的工程潜力,研究团队分别以对铜和锌响应的双组分系统为例,对原型的TCS进行“解耦”与“重编程”(图2A)。他们敲除了大肠杆菌(E. coli)基因组中内源的TCS,利用两个正交的诱导型启动子分别控制HK和RR的表达,实现了对两者浓度的精细、连续调控(图2B)。研究发现,即使在无目标信号刺激时,仅提高RR的浓度,就能将报告基因的表达水平最高提升502倍,展现出浓度依赖的强效激活作用;相反,增加HK的浓度,能降低表达水平最高达91倍(图2C,D)。这一发现突破了传统认知中TCS输出对HK和RR浓度不敏感的固有观念。为了证明其普适性,研究团队不仅建立了严谨的数学模型(图2E),还对大肠杆菌中近半数的TCS进行了系统的实验验证,充分证实RR和HK可作为广泛适用的“基因表达调控旋钮”,为基础研究与合成生物学应用提供了全新的调控维度。
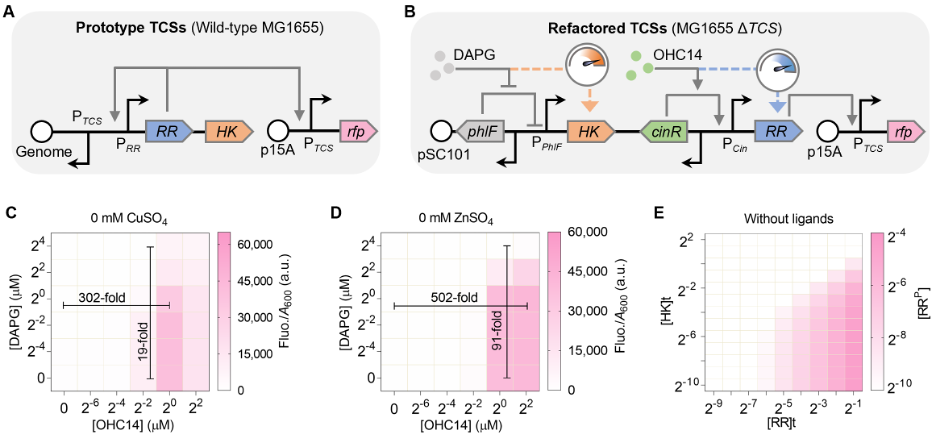
基于上述发现,研究团队展开了一系列合成生物学设计,将理论突破转化为强大的应用工具。
1. 构建“类开关型”超灵敏传感线路
在天然的TCS中,RR的正反馈激活通常与HK的负向抑制相互掣肘。研究团队通过理性重构,设计了一种“去耦合的正反馈回路”:让RR的表达受其自身激活的启动子控制(形成强正反馈),而HK则由组成型启动子恒定、适量表达(避免过度抑制)(图3A)。通过使用不同强度的核糖体结合位点(RBS)精细调节RR的表达水平,成功获得了具有超灵敏、开关式(YES/NO)激活响应的传感器(图3B,C)。重要的是,通过调节HK的表达水平,可以线性地改变传感器的灵敏度(K1/2),使传感器灵敏度可调(图3D-F)。
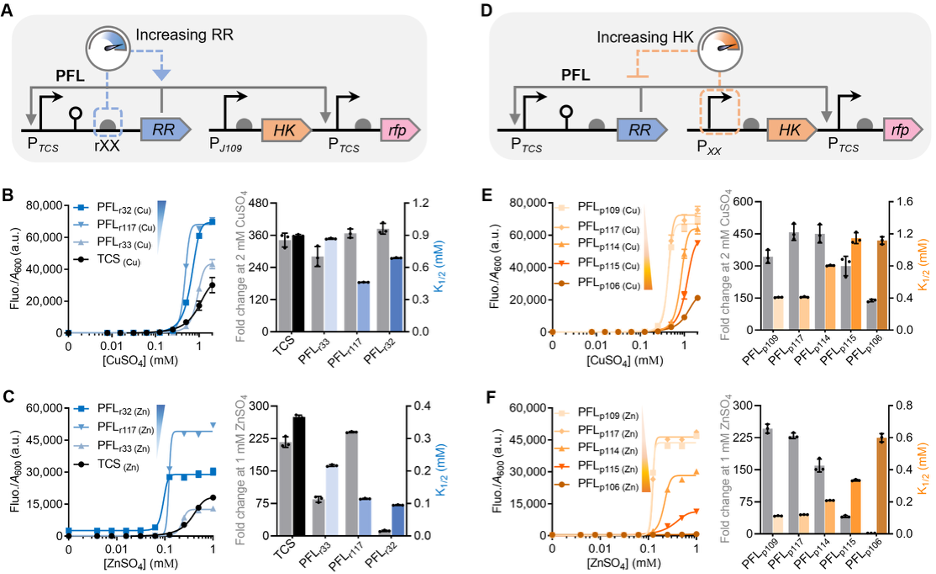
2. 创造“优势融合”的协同感应系统
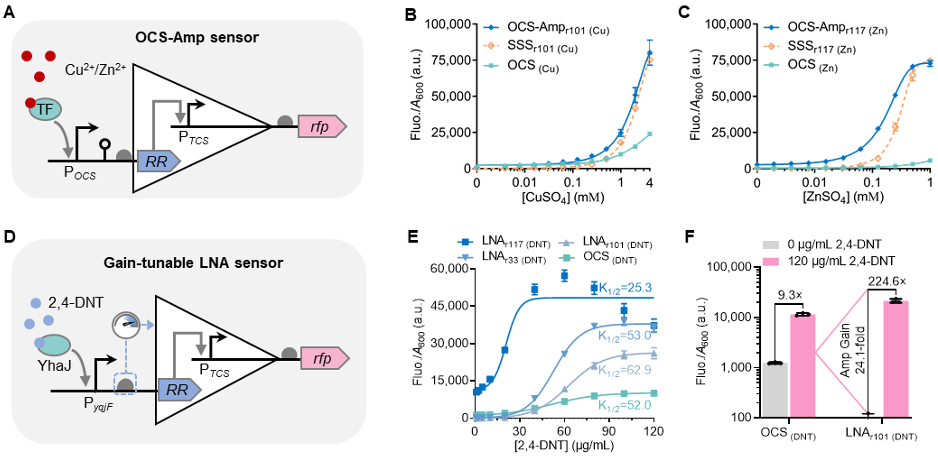
研究团队发现铜和锌响应的OCS通常检测限更低,但泄漏表达高;TCS则动态范围更广,信噪比出色(图4A-C)。能否取长补短?他们创新性地以RR为信号转导器,将OCS模块与TCS模块串联,构建了“协同感应系统“(图4D)。在这个系统中,OCS的转录因子负责高灵敏度的痕量信号感知,并启动RR的表达;随后,RR与组成型表达的HK共同构成TCS传感器,驱动高强度的信号输出。最终该系统同时兼具了OCS的低检测限和TCS的高动态范围(超过200倍),实现了传感性能的优势融合(图4E,F)。
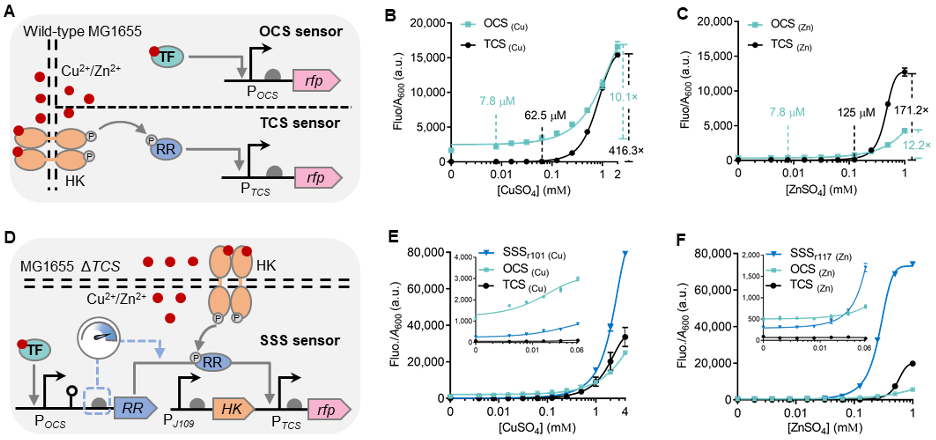
3. 开发“即插即用”的低噪音放大器
最令人惊奇的发现是:RR自身就是一个高性能的放大器模块。研究团队移除了协同感应系统中的HK,仅保留RR来放大OCS的输出信号,结果这种简化的“OCS-Amp”电路表现优异(图5A-C)。他们进一步将这一放大器工具“通用化”,成功应用于砷、2,4-二硝基甲苯响应的单组分传感系统和氮氧化三甲胺、硝酸盐响应的双组分传感系统中。仅通过简单地将目标传感器的输出与RR表达耦合,就使原始传感器的信号动态范围提升了4.0~24.1倍,同时保持了极低的泄漏表达(图5D-F)。与传统的转录放大器相比,研究团队基于锌离子双组分系统的RR(ZraR)开发的低噪音放大器具有更强的模块性和信号放大能力,可广泛兼容于各种基于转录/翻译控制的生物传感体系。
总之,这项研究不仅通过实验和数学模型系统揭示了TCS组分在工程化条件下的高度可塑性,更将其转化为一套从“原理”到“设计”的定量化工具手册。它使得研究者能像工程师调试电路一样,通过调节“RR”和“HK”这两个旋钮,精准设定传感器的灵敏度与信号输出强度。鉴于TCS在微生物界广泛存在,挖掘并重编程各类高性能、适用于不同底盘的TCS,将为生物诊断、环境监测与生物制造等领域,提供性能更强、应用更广泛的全新工具箱。
论文信息
Chen S#, Xu H#, Wan X, Zhang Y, Li Y, Zhou N*, Wang B** and Ye B*, “Refactoring two component systems for tunable gene expression regulation and upraded bacterial sensing”, Cell Systems, 2026, 17(3), 101504. doi (**lead contact)